Yuanfeng POV: Cronograma atualizado da EUDAMED
A Comissão da UE anunciou recentemente atualizações para a conclusão e aplicação do EUDAMED com base na alteração 2024/1860.Este artigo descreve os cronogramas actuais da EUDAMED e o nosso ponto de vista sobre estes cronogramas para ajudar a indústria a preparar-se em conformidade.
Calendários atuais da EUDAMED:
- A data-limite para a primeira aplicação obrigatória dos módulos funcionais EUDAMED é ainda 1 de janeiro de 2026.O módulo de vigilância deverá ser obrigatório a partir do terceiro trimestre de 2026, com a plena funcionalidade do EUDAMED prevista para o segundo trimestre de 2027..
- Os módulos Actor, UDI & Devices, Certificates e Market Surveillance estão actualmente sob auditoria.A auditoria independente do produto mínimo viável (MVP) destina-se a avaliar e confirmar a funcionalidade e a interconectividade dos módulos considerados prontos para auditoria.Esta auditoria deverá ser concluída no segundo trimestre de 2025.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Espera-se que os módulos Actor, UDI & Devices, Certificates e Market Surveillance sejam declarados totalmente funcionais no final do segundo trimestre de 2025, levando à sua data de aplicação obrigatória de 1 de janeiro. 2026.
- Não. - Espera-se que os módulos Actor, UDI & Devices, Certificates e Market Surveillance sejam declarados plenamente funcionais até ao final do segundo trimestre de 2025 e obrigatórios para uso industrial em 1 de janeiro de 2026.
- O módulo de vigilância não faz parte da auditoria MVP em curso e não será declarado plenamente funcional juntamente com os módulos mencionados anteriormente.O calendário revisto indica que a auditoria desse módulo ocorrerá entre o segundo e o terceiro trimestre de 2025, com o objetivo de que a data de aplicação obrigatória seja o segundo trimestre de 2026.
- Não. - O desenvolvimento do módulo de Investigação Clínica/Estudos de Desempenho (CI/PS) deverá continuar até ao terceiro trimestre de 2026.Uma auditoria para avaliar o módulo CI/PS, juntamente com os outros cinco (5) módulos, será concluída uma vez desenvolvido o MVP CI/PS.
- Não.
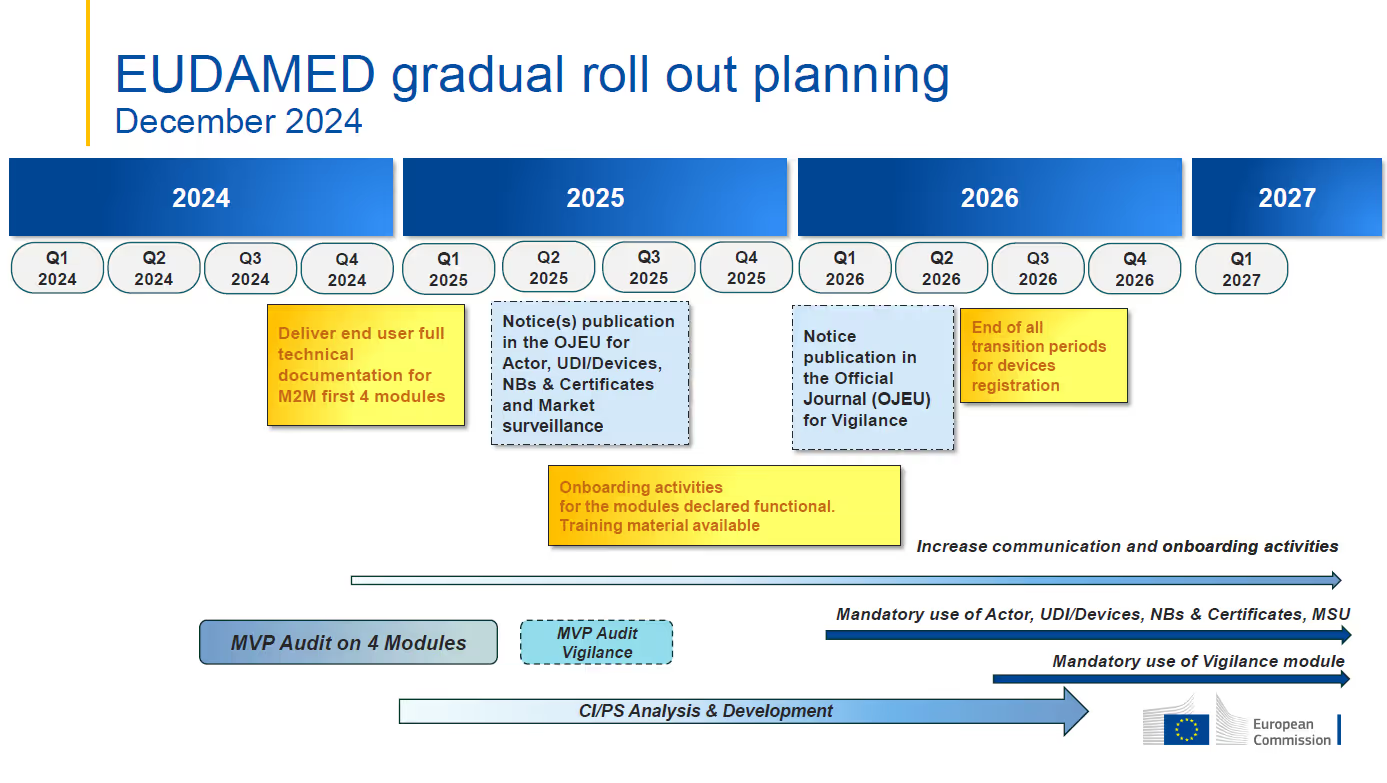
Foto cortesia doComissão Europeia
A Comissão da UE anunciou recentemente actualizações para a conclusão e implementação do EUDAMED com basealteração 2024/1860.Este artigo descreve os cronogramas actuais da EUDAMED e o nosso ponto de vista sobre estes cronogramas para ajudar a indústria a preparar-se em conformidade.
Calendários atuais da EUDAMED:
- A data-limite para a primeira aplicação obrigatória dos módulos funcionais EUDAMED é ainda 1 de janeiro de 2026.O módulo de vigilância deverá ser obrigatório a partir do terceiro trimestre de 2026, com a plena funcionalidade do EUDAMED prevista para o segundo trimestre de 2027..
- Os módulos Actor, UDI & Devices, Certificates e Market Surveillance estão actualmente sob auditoria.A auditoria independente do produto mínimo viável (MVP) destina-se a avaliar e confirmar a funcionalidade e a interconectividade dos módulos considerados prontos para auditoria.Esta auditoria deverá ser concluída no segundo trimestre de 2025.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Espera-se que os módulos Actor, UDI & Devices, Certificates e Market Surveillance sejam declarados totalmente funcionais no final do segundo trimestre de 2025, levando à sua data de aplicação obrigatória de 1 de janeiro. 2026.
- Não. - Espera-se que os módulos Actor, UDI & Devices, Certificates e Market Surveillance sejam declarados plenamente funcionais até ao final do segundo trimestre de 2025 e obrigatórios para uso industrial em 1 de janeiro de 2026.
- O módulo de vigilância não faz parte da auditoria MVP em curso e não será declarado plenamente funcional juntamente com os módulos mencionados anteriormente.O calendário revisto indica que a auditoria desse módulo ocorrerá entre o segundo e o terceiro trimestre de 2025, com o objetivo de que a data de aplicação obrigatória seja o segundo trimestre de 2026.
- Não. - O desenvolvimento do módulo de Investigação Clínica/Estudos de Desempenho (CI/PS) deverá continuar até ao terceiro trimestre de 2026.Uma auditoria para avaliar o módulo CI/PS, juntamente com os outros cinco (5) módulos, será concluída uma vez desenvolvido o MVP CI/PS.
- Não.

Foto cortesia doComissão Europeia
Eis como a Rimsys vê o impacto deste anúncio para cada grupo de partes interessadas:
Yuanfeng
A UDI está na frente da mente, assim como a interação futura com o módulo de vigilância.A Rimsys continuará a desenvolver a funcionalidade UDI e de vigilância pós-comercial independentemente das datas-alvo atualizadas.Reconhecemos igualmente o impacto potencial do estabelecimento de capacidades de transferência de dados (DTX) para interagir com o EUDAMED numa capacidade de máquina a máquina (M2M).Com a publicação dos requisitos finais necessários para o M2M DTX ao EUDAMED, a Rimsys está posicionada para finalizar a nossa ligação e oferecer capacidades M2M como parte da solução EUDAMED.
Indústria/cliente
Uma vez que a Comissão Europeia atualizou repetidamente os prazos da EUDAMED, esperamos que a indústria tenha alguma relutância em aceitar as novas datas-alvo.Isto pode atrasar o re-engajamento com os preparativos da EUDAMEDNo entanto, não esperamos que a CE empurre estes prazos atualizados.Os fabricantes que não tenham um plano para apresentar dados ao EUDAMED até ao segundo trimestre deste ano deverão esperar desafios significativos para cumprir estes prazos.Com a auditoria dos módulos esperados em curso e a documentação técnica associada publicada,A Rimsys recomenda que sejam tomadas medidas para organizar os dados regulamentares agora e submeter as suas informações precocemente a todos os módulos EUDAMED disponíveis..
Comissão da UE
A CE recomenda vivamente que a indústria continue a desenvolver a sua solução e a apresentar dados numa base voluntária.A posição da Comissão é de que a apresentação precoce de dados dará às empresas uma vantagem, pois os seus dados estarão à frente do ataque de toda a indústria mundial da MedTech.As empresas que pretendem adicionar dados ao mesmo tempo que o EUDAMED se torna obrigatório, estarão também na linha de frente para trabalhar com os recursos da Comissão se surgirem problemas de apresentação de dados.
* Nota - este artigo inclui interpretações regulamentares e pareceres doYuanfengA Comissão Europeia e os Estados-Membros têm a obrigação de fornecer informações sobre as medidas a tomar para garantir a segurança e a segurança dos transportes.

